2024年1月8日,中国科学技术大学生命科学与医学部周江宁教授团队在Translational Neurodegeneration上发表了最新研究成果“Increased cysteinyl-tRNA synthetase drives neuroinflammation in Alzheimer's disease”,揭示了半胱氨酰-tRNA合成酶(CARS)失调诱发的神经炎症参与阿尔茨海默病发病的机制。
阿尔茨海默病(Alzheimer’s Disease, AD)是一种以记忆力减退和认知功能障碍为主要临床表现的神经退行性疾病,是最常见的痴呆症类型。目前,全世界超过5500万人患有痴呆,每年有近1000万新增病例。阿尔茨海默病已成为危害生命健康和加重社会负担的公共问题。神经炎症是中枢神经系统中由胶质细胞激活的免疫应答。近年来研究发现神经炎症反应在AD发生和发展过程中起了关键作用。CARS作为一种氨酰-tRNA合成酶,主要负责将半胱氨酸(Cysteine, Cys)与同源tRNAcys配对和连接,形成相应的氨酰-tRNA。氨酰-tRNA的正确形成决定了蛋白质合成的整体保真度。CARS同时也是内源的免疫刺激因子,在病理条件下可以激活机体产生免疫应答反应。最新的研究显示,CARS基因突变会引起运动功能障碍和认知损伤,但其在阿尔茨海默病的作用还不清楚。
在本研究中,研究人员首先利用免疫组化和分子生物学方法对人脑组织样本进行了检测,发现AD病人脑颞叶皮层中的CARS免疫反应性和蛋白水平显著提高,其中早期AD病人脑颞叶皮层的CARS表达水平最高。进一步的研究结果显示,CARS 在人脑皮层神经元中富集,神经元表达的CARS 水平在AD病人脑颞叶皮层中显著上调。利用腺相关病毒介导的基因过表达方法,在正常C57BL/6J小鼠或APP/PS1双转基因AD小鼠海马脑区神经元内过表达CARS,可引起/加剧小鼠的认知功能缺陷,伴随着海马小胶质细胞的激活,Toll样受体2(TLR2)和髓样分化因子88(MyD88)蛋白表达的升高以及神经炎症因子水平的上调。体外细胞实验进一步验证了小鼠的实验结果,CARS处理BV2小胶质细胞可引起趋化反应,激活TLR2/MyD88信号通路,导致肿瘤坏死因子-α(TNF-α)等促炎细胞因子释放增加。利用TNF-α处理SHSY5Y神经细胞,引起了CARS 的胞内表达和胞外分泌增加。上述结果显示神经元来源的CARS,小胶质细胞和炎症因子之间形成了一个正反馈循环,引发/加剧了神经炎症,导致认知功能缺陷(详见图解)。最后研究人员发现在AD病人脑中,CARS 在伴有神经炎症的致密核心型 β 淀粉样蛋白(Aβ)斑块中聚集,提示CARS诱导的神经炎症可能是AD发生和发展的重要诱因。
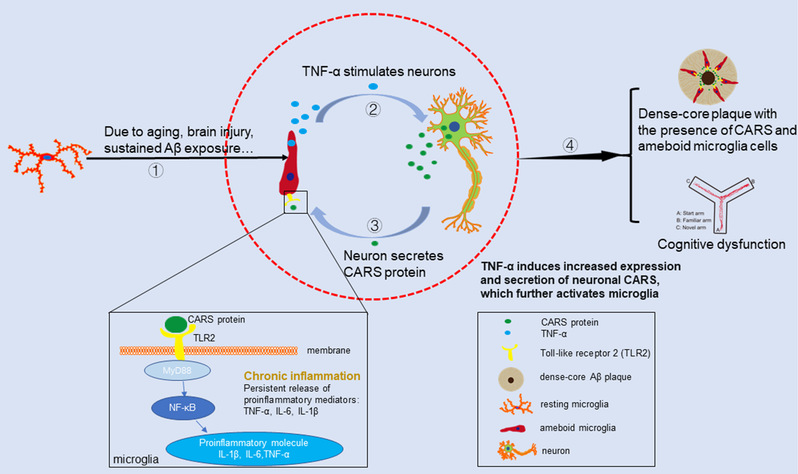
该项研究首次揭示了半胱氨酰-tRNA合成酶CARS在大脑中的全新功能,阐明了神经元来源的CARS失调诱发的神经炎症参与阿尔茨海默病发病的新机制,为寻找AD的潜在干预靶点提供了神经生物学依据。
中国科学技术大学博士后戚秀红和安徽医科大学第一附属医院陈鹏教授为论文的共同第一作者,周江宁教授为唯一通讯作者。中国科学技术大学为论文第一单位。本研究得到了苏州大学附属第一医院王月菊主任医师,协和医科大学北京协和医院张振馨教授和中国科学技术大学刘际研究员的大力帮助。该项工作得到了中科院B类先导、科技创新2030-“脑科学与类脑研究”重大项目和国家自然科学基金等项目资助。
文章链接:
tps://translationalneurodhtegeneration.biomedcentral.com/articles/10.1186/s40035-023-00394-6
