近日,中国科学技术大学钱洪武教授课题组在《Nature Communications》期刊在线发表了题为“Structural basis for cholesterol sensing of LYCHOS and its interaction with indoxyl sulfate”的研究论文,解析了人源LYCHOS蛋白感知溶酶体胆固醇的结构基础,并揭示了其与肠源性毒素分子硫酸吲哚(indoxyl sulfate, IS)的结合机制。
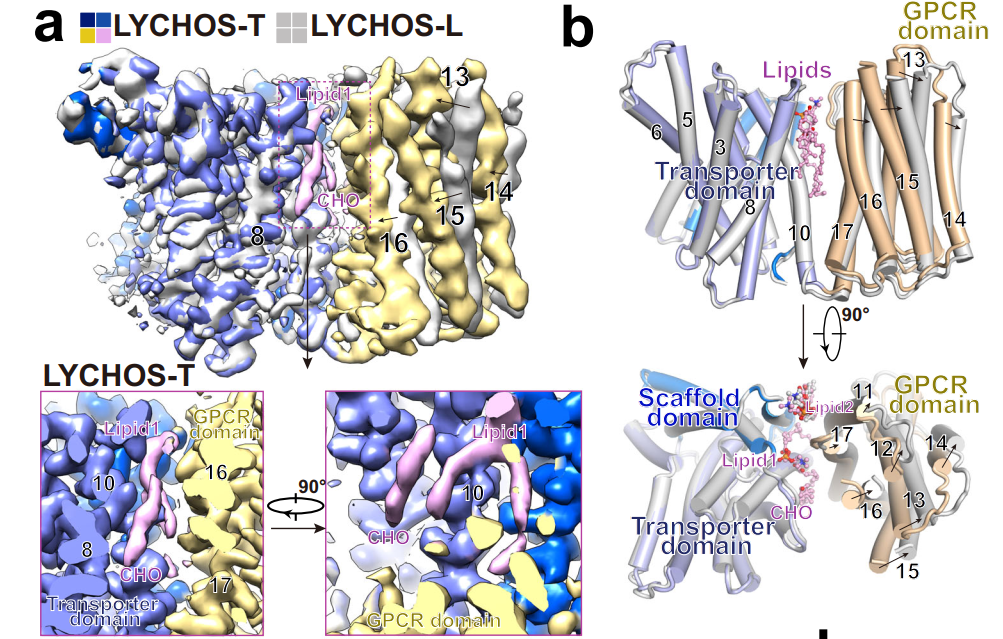
图1 LYCHOS感知胆固醇的结构基础
LYCHOS是定位于溶酶体的膜蛋白,由氨基端的转运结构域和羧基端的GPCR结构域组成。LYCHOS可以感知溶酶体胆固醇水平,从而激活mTORC1信号通路。然而,该蛋白识别胆固醇信号的分子机制此前尚不明确。中国科学技术大学钱洪武团队利用冷冻电镜(cryo-EM)技术,成功解析了人源LYCHOS蛋白高分辨率结构,发现了转运结构域和GPCR结构域相互作用界面的胆固醇结合位点。进一步通过解析该蛋白在不同胆固醇结合状态下的构象,发现了胆固醇可以诱导两个结构域相互靠近,揭示了LYCHOS感知胆固醇水平的结构基础(图1)。
此外,该研究还进一步探究了该蛋白转运结构域的转运底物。通过筛选发现,LYCHOS的转运结构域可以结合硫酸吲哚(IS)。IS是吲哚类衍生物,是一类肠源性毒素分子,与慢性肾病和心血管疾病密切相关。后续该团队通过结构生物学手段阐明了转运结构域与IS分子的结合方式,并利用相互作用实验进行了验证(图2)。然而LYCHOS转运结构域是否可以转运IS尚需进一步的研究。
总结而言,该项工作揭示了LYCHOS感知胆固醇水平的结构基础,加深了领域内对于胆固醇调节mTORC1信号通路的理解。还发现了与LYCHOS相互作用的其他代谢分子,为后续LYCHOS的功能研究提供了新思路。中国科大钱洪武教授为该论文的通讯作者,中国科大博士后王振华、博士生何晶晶为该论文的共同第一作者。该研究得到国家自然科学基金、科大双一流建设经费等项目的支持。
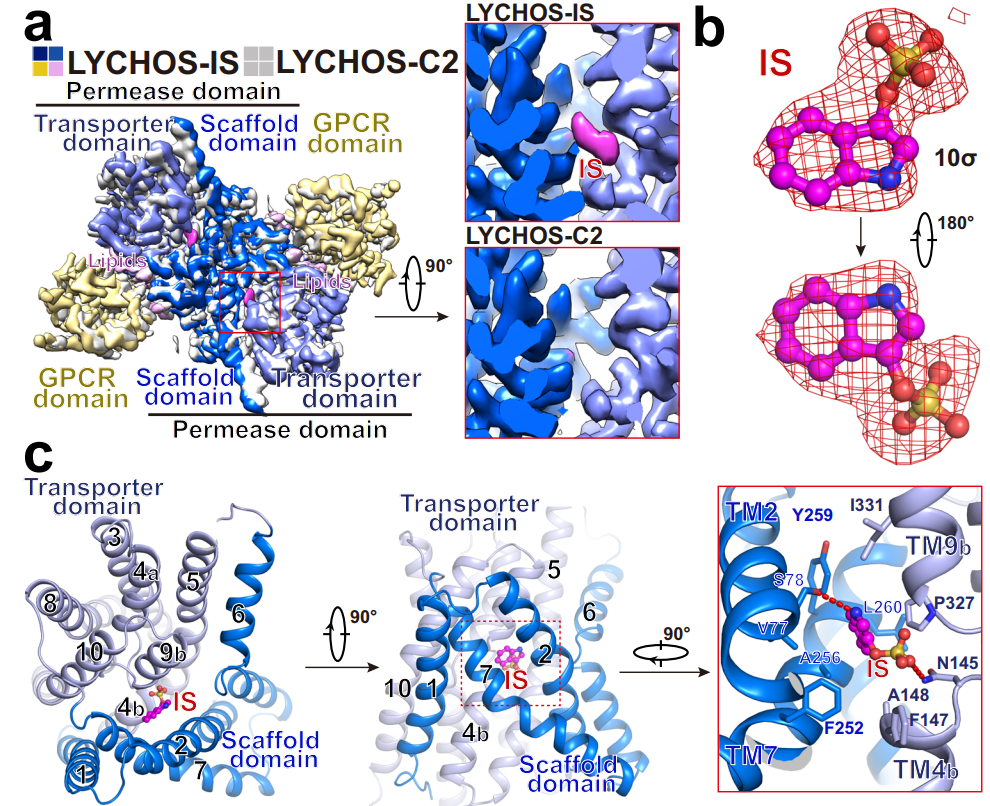
图2 LYCHOS转运结构域与硫酸吲哚(IS)的结合机制
论文链接:https://www.nature.com/articles/s41467-025-58087-9
