近日,中国科学技术大学王育才/李敏团队在《Nature biomedical engineering》杂志在线发表了一篇题为“Generation of tolerogenic antigen-presenting cells in vivo via the delivery of mRNA encoding PDL1 within lipid nanoparticles”的研究论文。该工作首创低免疫原性LNPs递送PD-L1 mRNA策略,成功在体内直接编程生成tol-APCs,治疗自身免疫性疾病。

自身免疫疾病(AIDs)的治疗一直面临着严峻挑战。其关键的病理机制在于,异常活化的T细胞会对宿主自身组织发起攻击。传统的治疗方法,例如单克隆抗体或者重组蛋白,虽然可以抑制T细胞的活性,但因其缺乏靶向性,常常会造成全身免疫抑制,进而引发严重的副作用。近年来,研究重点逐渐转移到了耐受性抗原呈递细胞(tol - APCs)上。这类细胞能够表达PD-L1等负性共刺激分子,可特异性地诱发病理性T细胞失能,或者促使其转化为具备免疫抑制功能的调节性T细胞(Treg)。然而,目前的技术需要从患者体内分离出抗原呈递细胞(APCs),然后在体外对其进行诱导和抗原加载。这种复杂的个体化操作流程成本极高,这在很大程度上阻碍了其在临床应用中的推广。
mRNA技术可通过编程蛋白表达,具有精准调控免疫反应的潜力,但其核心递送载体脂质纳米颗粒(LNPs)因固有免疫刺激性,会激活APCs并触发炎症反应,与AIDs治疗所需的免疫耐受目标相矛盾。因此,开发同时具备低免疫原性和能够精准靶向APCs的mRNA递送系统,是实现mRNA免疫耐受疗法的核心。团队通过对LNPs的氮磷比(N/P比)和组分配比进行系统性优化,筛选出了较低免疫原性的LNPs。这些LNPs能够有效性递送编码PD-L1的mRNA至APCs,使其高效表达PD-L1,且不会引发炎症反应。在类风湿性关节炎(RA)和溃疡性结肠炎(UC)的模型里,体内生成的tol-APCs借助PDL1 - PD1的相互作用,有选择性地抑制过度活化的致病性T细胞,同时使调节性T细胞(Treg)扩增,从而显著抑制了疾病的进展。该团队首次将mRNA技术从预防性疫苗、肿瘤治疗领域拓展到了自身免疫疾病领域,在基于mRNA技术在体内细胞编程嵌合抗原受体T细胞(CAR-T)模式,开辟了“体内耐受性免疫细胞工程”这一新思路。
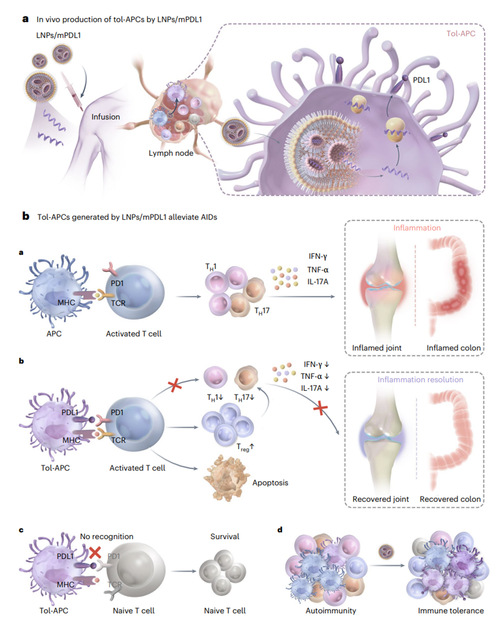
示意图:低免疫原性递送mRNA生成tol-APCs用于自身免疫性疾病治疗。
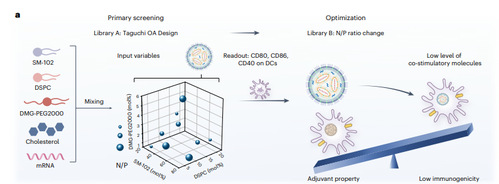
传统mRNA递送系统(如COVID-19疫苗使用的LNPs)通过激活APCs表面的共刺激分子(CD80/CD86/CD40)介导强效免疫应答。为解决这一问题,研究团队采用实验设计(DOE)系统调整LNPs的四种组分(SM-102、DSPC、DMG-PEG2000、胆固醇)的摩尔比例与N/P比,构建LNPs库。通过两轮活体筛选,确定了具有低免疫原性、高表达效率的LNP配方。该配方和商用配方相比显著降低APC表面共刺激分子CD80/CD86/CD40的表达水平,同时保持转染效率稳定。
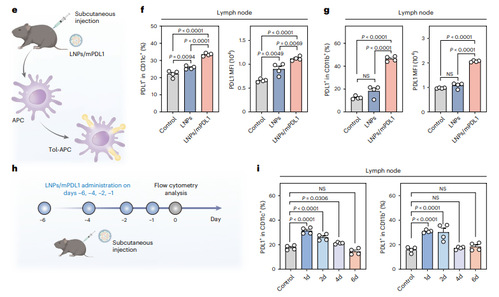
使用该配方LNPs封装编码PDL1的mRNA(LNPs/mPDL1),并经小鼠皮下注射后,淋巴结CD11c+和CD11b+细胞PDL1表达显著升高,说明了tol-APCs的成功生成,而骨髓中未检测到tol-APCs生成,且LNPs/mPDL1对非APC的免疫细胞影响极小,表明经优化的LNPs成功实现低免疫原性递送PDL1 mRNA至APCs,实现tol-APCs的在体生成。
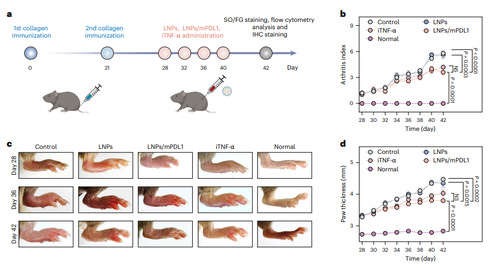
在上述基础上,研究团队搭建Ⅱ型胶原免疫诱导的RA模型里,以此来验证LNPs/mPDL1的治疗效果。当这些小鼠接受LNPs/mPDL1治疗之后,通过评估发现其关节肿胀评分明显下降。通过番红固绿染色及滑膜免疫组化分析发现,LNPs/mPDL1治疗显著缓解了胶原诱导性关节炎(CIA)小鼠的病理进展:其软骨损伤程度恢复至接近正常水平,滑膜组织中促炎因子IFN-γ和TNF-α表达显著降低,CD8⁺、CD4⁺ T细胞浸润减少,同时调节性T细胞(Tregs)比例升高,表明治疗有效重塑了免疫稳态。此外,关节炎症评分显示LNPs/mPDL1的抗炎效果与TNF-α抑制剂依那西普相当,进一步证实该疗法通过靶向调控T细胞亚群及炎症微环境,在抑制自身免疫反应、促进软骨修复及骨保护方面展现出与现有临床疗法相当的潜力。
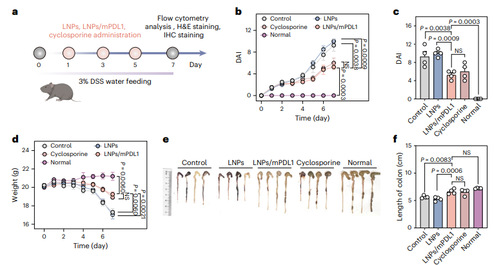
随后,研究团队对LNPs/mPDL1在UC模型中的治疗效果展开了评估。研究中,采用葡聚糖硫酸钠(DSS)诱导C57BL/6小鼠,这些小鼠出现了严重的结肠缩短现象,平均结肠长度仅为5.6厘米,同时伴有明显的黏膜损伤。然而,接受LNPs/mPDL1治疗的小鼠,其结肠长度恢复到了正常水平,达到6.6厘米,并且结肠黏膜结构完整,隐窝破坏情况得到显著缓解。值得注意的是,其治疗效果与使用环孢素的效果相当。进一步研究发现,LNPs/mPDL1治疗使得肠道炎症部位的CD4⁺和CD8⁺ T细胞浸润显著减少,调节性T细胞(Treg)数量增加,同时肿瘤坏死因子 - α(TNF - α)水平降低。此外,研究团队还观察到,LNPs/mPDL1显著降低了肠系膜、腹股沟淋巴结、脾脏以及血液中的效应T细胞数量。
综上所述,团队通过优化LNPs的N/P比与脂质组成,显著降低载体免疫原性,使APCs特异性高表达PD-L1的同时维持低水平的共刺激分子表达,选择性的抑制致病性T细胞活性并扩增Treg。在RA和UC模型中,其疗效优于临床标准药物依那西普与环孢素,且单次治疗成本不足传统体外细胞疗法的1%,兼具高效性与经济性。研究突破传统疗法的三大局限:无需体外操作,皮下注射直接靶向APCs;广谱适应,非抗原特异性模式适用于致病抗原不明的自身免疫病(如UC),而加载特定抗原可拓展至多发性硬化症等疾病;平台化扩展,未来可整合CTLA-4等共抑制分子或趋化受体增强疗效,或通过肝靶向递送诱导移植免疫耐受。此项成果以“体内细胞编程”理念,潜在的为多种自身免疫性疾病以及器官移植提供全新范式。
中国科学技术大学刘洋博士、刘潜博士、博士生张宝文为该论文共同第一作者,中国科学技术大学王育才教授、李敏副教授为本文共同通讯作者;团队其他成员及合作者也为本研究做出了重要贡献。
论文链接:https://www.nature.com/articles/s41551-025-01373-0
