随着工业化进程加快,IBD已成为重大慢性疾病。尽管抗TNFα、IL-12/23p40等生物制剂有效缓解炎症,但原发不响应、继发失效和高复发率仍是临床难题。越来越多证据表明,真正决定长期预后的不是单纯炎症控制,而是黏膜是否实现有效愈合,而上皮修复是核心环节。然而,在炎症微环境中,上皮修复常被异常抑制,其分子机制和可干预靶点仍不清晰。
2026年2月23日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗全国重点实验室潘文教授团队在Cell Stem Cell发表论文“VIPR1 acts as an enteric neural checkpoint that suppresses intestinal stem cell-driven epithelial regeneration and exacerbates colitis”,首次提出调控肠道上皮修复再生的“神经检查点”机制。研究揭示,在炎症性肠病 (IBD) 等慢性炎症中,VIP能神经元通过直接激活干细胞受体VIPR1,抑制上皮再生程序,延缓黏膜愈合并加重炎症进展,确立了神经系统对肠道上皮修复的关键门控作用。

此前,团队于2024年6月在Cell Host & Microbe报道,肠炎相关肠球菌产生的酪胺(tyramine)可激活干细胞表面α2A肾上腺素能受体,抑制上皮修复、延缓黏膜愈合并加重炎症。应用α2A受体选择性拮抗剂Yohimbine可阻断这一抑制效应,显著促进上皮修复并缓解肠炎,体现了“老药新用”的潜在转化价值(详见BioArt报道:专家点评Cell Host Microbe | 潘文/朱书/宋昕阳发现肠球菌抑制肠道干细胞增殖加重肠炎的机制及干预方法)。
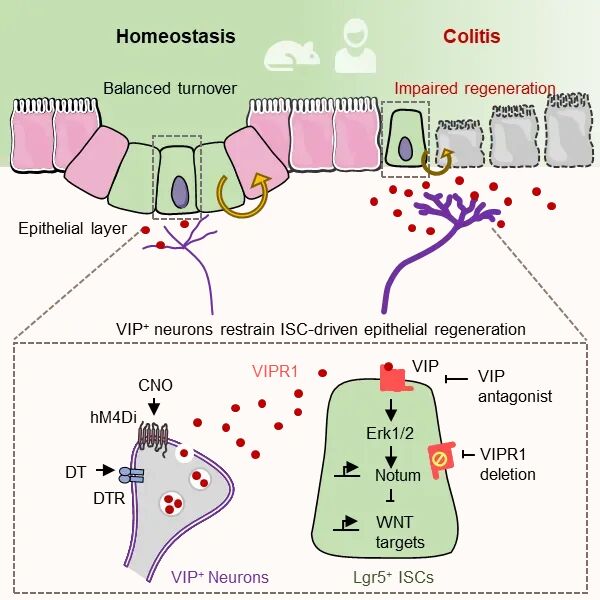
在此基础上,本研究进一步聚焦神经来源信号。肠道上皮作为多系统信号交汇的界面组织,持续接受外周神经调控,但神经信号是否构成上皮修复再生的关键调控因素及其在肠炎损伤修复中的机制,长期未明。团队依托类器官平台和多种体内遗传调控手段,系统解析了VIP能神经元在炎症背景下对上皮再生的抑制作用。结果表明,VIP信号通过VIPR1-ERK-Notum轴调控干细胞WNT通路,精细调节炎症期上皮损伤与修复模式;多时间点、多基因标记分析描绘了炎症过程中上皮修复的动态轨迹;多重基因干预实验进一步证实,阻断该神经抑制轴可显著恢复上皮修复能力,加速黏膜愈合并缓解肠炎表型。
该研究系统揭示了神经系统对上皮修复的抑制性调控机制,为提升黏膜愈合率、开发新型促修复干预策略提供了明确的理论基础和潜在转化方向。
中国科大潘文教授为文章的通讯作者,博士后李朝亮和博士生王好好为本工作的共同第一作者。这个工作也获得多位合作者的大力帮助:中国科大附属第一医院消化科张开光主任提供了IBD病人组织样本;中国科大朱书教授和周荣斌教授也提供了实验支持和指导意见。
原文链接:https://www.cell.com/cell-stem-cell/abstract/S1934-5909(26)00032-9
