肝细胞癌(HCC)是全球第六大常见癌症和第三大癌症相关死亡原因,5年生存率仅约 18%。免疫检查点抑制剂(如 PD-1/PD-L1 抗体)为晚期肝癌治疗带来突破,但响应率仅 20%-30%。这种肿瘤微环境中免疫细胞功能失调机制尚不完全清楚。NK 细胞作为先天免疫的核心效应细胞,占肝癌肿瘤浸润淋巴细胞的 30% 左右,其功能受损与肿瘤进展密切相关。因此,深入解析HCC微环境中NK细胞功能失调的分子机制,寻找靶向性的NK细胞检查点,对于开发新的HCC免疫治疗策略具有重要的理论和临床意义。
2026年2月21日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗全国重点实验室孙成教授团队在《Nature Communications》发表论文“SAMSN1 restrains NK cell mediated anti-tumor immunity in hepatocellular carcinoma”。该研究首次证实SAMSN1蛋白作为NK细胞免疫检查点分子,其主要功能是抑制HCC中NK细胞的抗肿瘤免疫活性。作者通过整合分析临床患者样本数据与临床前动物模型,系统地揭示了SAMSN1在HCC进展中的关键作用及其作用机制。

研究团队首先利用已发表的单细胞测序(scRNA-seq)数据分析发现,与癌旁组织(PT)相比,HCC患者瘤内区域(IT)的NK细胞中SAMSN1的表达显著上调。此外,生存分析显示,无论是在公共数据库(TCGA cohort)还是该研究自身的患者队列中,肿瘤组织或NK细胞中高表达的SAMSN1均与患者较差的总体生存率和无病生存率显著相关,提示SAMSN1可能诱导HCC中肿瘤浸润NK细胞的功能耗竭。
为了验证SAMSN1对NK细胞功能的直接影响,研究团队在体外使用基因敲除技术敲除了原代人NK细胞中的SAMSN1并进行相应的分析。结果显示,敲除SAMSN1后,NK细胞的活化标志物表达上调,抑制性受体表达下降,且基因富集分析证实,敲除效应与“NK细胞活化正调控”等通路显著相关。在NK92细胞系中进行的过表达和敲除实验进一步表明,SAMSN1对NK细胞的抑制功能。此外,研究通过代谢分析发现,过表达SAMSN1的NK92细胞氧耗率降低,细胞外酸化率升高,表明其代谢状态向糖酵解偏移,这可能是其功能受损的代谢基础。
通过动物模型研究发现,与野生型小鼠相比Samsn1基因敲除小鼠在Hepa1-6肝原位模型中的肿瘤生长明显抑制同时小鼠生存期显著延长。通过深入研究发现,这种抗肿瘤效应伴随着瘤内NK细胞功能的显著增强,敲除小鼠中肿瘤浸润性NK细胞分泌GZMB和IFN-γ的水平显著增强。为了更精确地证明SAMSN1的作用是NK细胞内在性的,团队构建了NK细胞特异性条件性敲除小鼠。当仅在NK细胞中敲除Samsn1时,其抗肿瘤表型与全局敲除小鼠高度一致:肿瘤负荷显著降低同时生存期显著延长。这一关键实验确证了SAMSN1主要通过抑制NK细胞自身功能来促进HCC进展,其作用具有细胞类型特异性。此外,在MC38结肠癌和B16F10黑色素瘤模型中的探索性实验也观察到类似现象,提示SAMSN1的免疫抑制功能可能不局限于HCC,在其它实体瘤中亦可能存在。
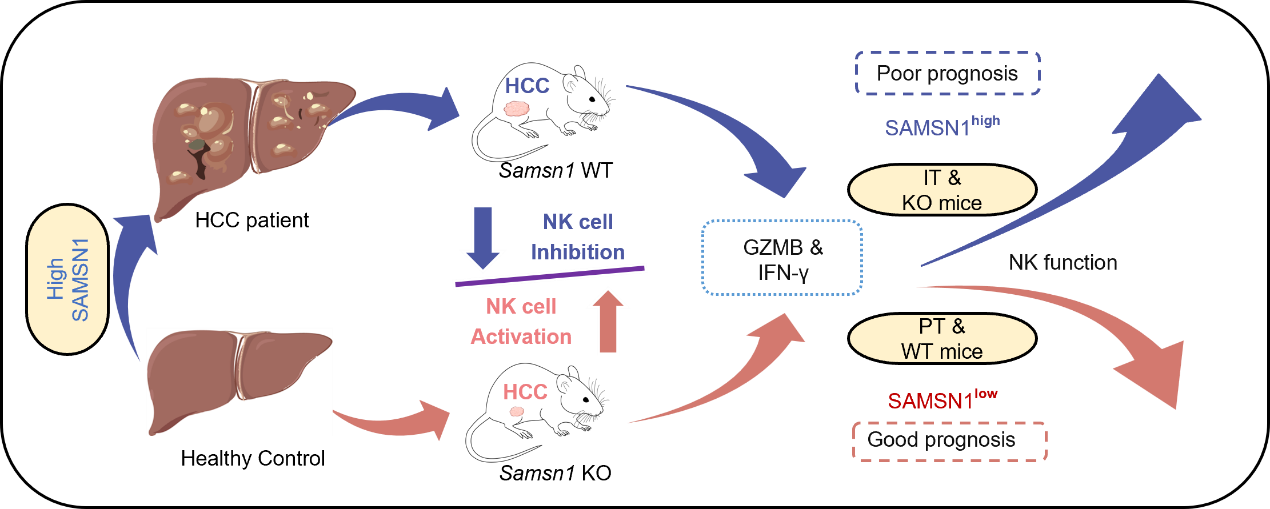
该研究从临床观察到机制探索,再到功能验证,提供了充分的证据链,将SAMSN1确立为一个全新的、作用机制明确的NK细胞检查点。其临床相关性体现在SAMSN1高表达与HCC患者不良预后的强关联性;其作用特异性体现在NK细胞条件性敲除足以复现全局敲除的抗肿瘤效果;其功能机制体现在SAMSN1能够抑制NK细胞的活化、增殖、细胞毒分子分泌并诱导其代谢重编程。这些发现不仅深化了对HCC免疫微环境,特别是NK细胞功能失调的理解,也为HCC的免疫治疗提供了新的潜在靶点。鉴于当前以T细胞为中心的免疫检查点抑制剂在HCC中疗效有限,靶向SAMSN1以解除NK细胞抑制、增强其固有抗肿瘤免疫,可能成为未来HCC免疫治疗一个有前景的新方向,尤其可能惠及那些对现有疗法不敏感的HCC患者。
中国科学技术大学孙成教授为本文共同通讯作者;王瑞峰博士后(中国科学技术大学)、陈徽迪(中国科学技术大学)为本文的共同第一作者。
原文链接:https://www.nature.com/articles/s41467-026-68661-4
