mRNA是遗传信息从DNA传递到蛋白质的关键媒介。在真核细胞中,mRNA在细胞核内合成后,必须经过严格的加工和质量控制,才能被高效、准确地运输至细胞质进行翻译。这一过程由多个蛋白复合物协同完成,其中TREX-2复合物作为锚定在核孔复合体上的“转运枢纽”,在mRNA核输出中发挥着关键作用。然而,TREX-2如何识别并释放成熟的mRNA颗粒(mRNP),长期以来一直是领域内的未解之谜。
近日,中国科学技术大学生命科学与医学部张晓峰课题组在Nature Communications发表题为《Molecular insights into mRNA export regulation by the human TREX-2 complex》的研究论文。该研究解析了TREX-2复合物与RNA解旋酶UAP56的关键相互作用,从而揭示了mRNA核输出过程中“出口开关”的分子机制,为理解真核生物基因表达调控提供了新的见解。
研究团队首先通过免疫沉淀-质谱联用(IP-MS)结合AlphaFold结构预测,发现UAP56与TREX-2存在微弱但特异的相互作用,随后利用Pull-down实验证明UAP56确实是TREX-2在mRNP上的“抓手”。利用重组表达和体外重构技术,研究团队成功组装了包含GANP、PCID2和DSS1的TREX-2核心模块(TREX-2M),并进一步获得了其与UAP56的复合物结构。结构分析发现,UAP56通过其N端两个高度保守的环状结构(Loop-1和Loop-2)特异性地结合TREX-2M,形成稳定的相互作用界面。此外,TREX-2亚基GANP的一个保守的Loop 插入到了UAP56的解旋酶结构域中,使其呈现开放构象。这些相互作用不仅实现了mRNP与核孔复合物的初步对接,更重要的是,TREX-2M能够显著激活UAP56的ATP酶活性,从而促进UAP56从mRNA上解离,为下游的核输出受体NXF1-NXT1的招募“腾出空间”。
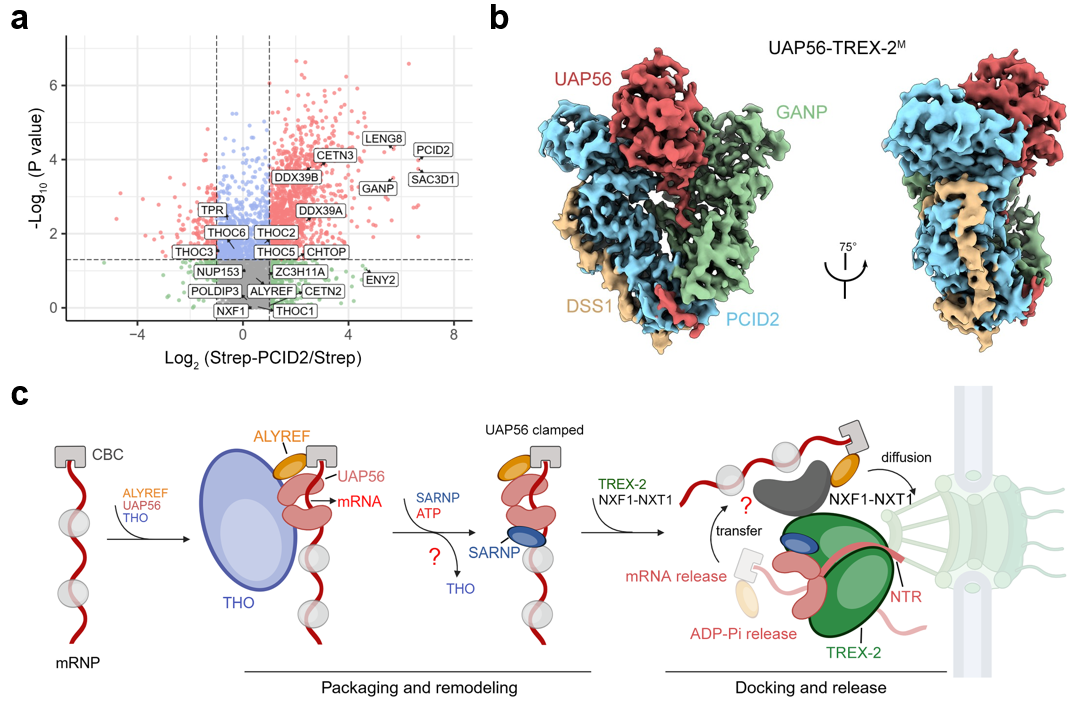
研究团队通过体外RNA释放实验验证了这一模型:当TREX-2M存在时,UAP56释放RNA的效率显著提高;而使用破坏UAP56-TREX-2M相互作用的突变体则明显削弱该效应。这些结果共同证明,TREX-2通过直接物理互作调控UAP56的构象和活性,进而促进mRNP从UAP56向NXF1-NXT1的“手递手”转移,实现了mRNA输出的关键步骤。
值得注意的是,该研究还揭示了这一调控机制在进化上的高度保守性。UAP56的N端调控模式与剪接体中的其他RNA解旋酶(如DDX42、DDX46)具有显著相似性,提示存在一种普适的重塑机制。此外,研究团队还发现,UAP56的同源蛋白URH49(DDX39A)虽也能与TREX-2微弱结合,但其亲和力远低于UAP56,表明TREX-2可能优先选择UAP56作为其功能适配器,以实现对mRNP的精准调控。未来,研究团队将进一步探索mRNA在不同生理与病理条件下的动态调控网络,致力于揭示mRNA核输出通路的全貌,助力开发靶向mRNA输出通路的新型诊疗策略。
中国科学技术大学博士生巩幸、陶然、朱慧慧以及澳门城市大学葛霄飞为论文共同第一作者。中国科学技术大学张晓峰和北京大学第三医院杭婧为论文的通讯作者。中国科学技术大学冷冻电镜中心高永翔博士为冷冻电镜数据采集提供了关键支持。该研究得到了国家自然科学基金、中国科学院引才计划青年项目、安徽省自然科学基金、合肥综合性国家科学中心大健康研究院项目的支持。
全文链接:https://www.nature.com/articles/s41467-026-70088-w
