2026年03月20日,中国科学技术大学生命科学与医学部王育才/朱书/蒋为课题组在Science期刊在线发表了题为“Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors”的研究论文。该研究突破传统“以材料为中心”的研究范式,基于宿主内源性免疫-代谢调控视角,系统揭示了一条由肠道共生菌驱动的肝免疫调控轴在体内递送系统(in vivo delivery systems,IDS)清除中的核心作用。研究发现,肠道微生物群能够重塑机体内分泌功能,持续促进吞噬刺激分子的释放,作用于肝脏吞噬细胞(Kupffer细胞),激活其特异性受体并诱导细胞骨架重塑及吞噬相关基因表达,从分子、形态及功能多个层级协同增强其清除能力。该调控机制不依赖于特定递送系统的材料组成、结构特征或载荷类型,对合成纳米载体及病毒载体均具有广泛适用性,体现出高度的系统性与普适性。通过短暂、可控地干预肠道菌群状态,可显著削弱肝脏对IDS的非特异性清除,在不破坏整体免疫稳态、引发系统性炎症的前提下,普遍提升多种IDS的体内递送效率。本研究建立了“肠道微生物—肝脏清除功能”的新理论框架,为突破体内递送效率与安全性瓶颈提供了具有普适性和临床转化潜力的全新调控策略。
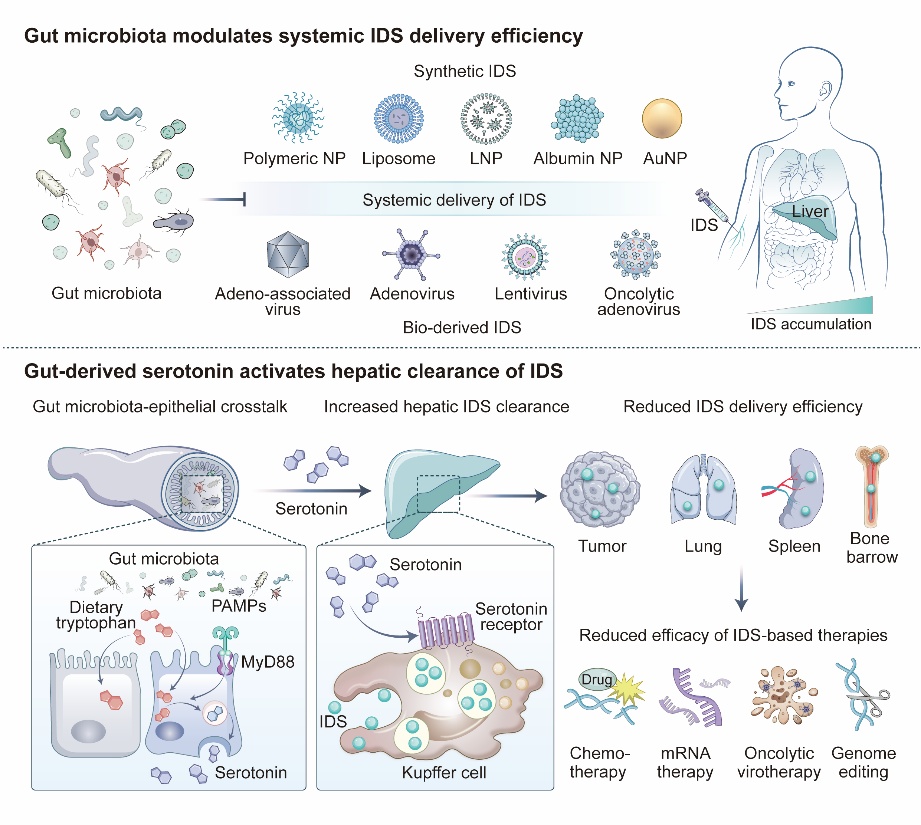
图1 肠道-肝脏免疫轴限制了基于IDS的治疗效果。肠道微生物群通过维持肝脏在稳态下的高水平清除功能,削弱了IDS在体内的循环。肠上皮将来源于微生物群的刺激信号传递至肝脏,其中血清素作为信使,驱动Kupffer细胞对IDS的吞噬。因此,仅有少量IDS能够到达靶组织,导致其在多种应用场景中的治疗效果不理想。NPs:纳米颗粒;LNPs:脂质纳米颗粒;PAMPs:病原体相关分子模式。
IDS是基因治疗、mRNA药物、体细胞基因编辑及精准肿瘤治疗实现临床转化的关键基础。尽管近年来在材料设计与工程优化方面取得系统性进展,其体内应用仍显著受制于过低的递送效率以及由此带来的靶向性不足和系统毒性高等问题。大量研究表明,上述问题并不能简单归因于载体材料性能不足,而在很大程度上归因于机体单核吞噬系统对外源递送载体的非特异性识别与快速清除。其中,肝脏作为机体最主要的清除器官,在IDS清除过程中占据主导地位。肝脏Kupffer细胞在稳态条件下维持高度活跃的吞噬功能,可清除大量IDS,导致其在到达靶组织前即被大量耗竭,显著削弱治疗效能并增加肝脏负担。针对这一长期制约递送领域发展的关键问题,现有策略主要集中于材料工程层面的优化,包括表面抗污修饰、仿生包裹、清道夫受体阻断或Kupffer细胞饱和等方式。然而,这些方法的递送效率提升幅度仍然受限,且在通用性、长期安全性及临床转化可行性方面存在明显不足,其根本原因在于对肝脏清除功能调控机制尚未得到系统阐明。因此,从宿主免疫与代谢调控层面解析其功能维持机制,是突破体内递送效率瓶颈的关键前提。
清除肠道微生物群或阻断细菌感知受体可显著降低肝脏清除作用,并提高多种IDS的递送效率,而不受其化学组成或负载类型的影响。这些改变显著增强了基于IDS的治疗效果,包括体细胞基因组编辑和精准肿瘤治疗。递送效率的提升归因于Kupffer细胞功能性失活,同时伴随其形态、分子表型及吞噬活性的显著改变。研究确定革兰阴性菌是该调控轴的主要驱动因素,但其并非通过细菌来源产物直接作用于Kupffer细胞。相反,肠道菌群通过调控肠上皮色氨酸代谢发挥作用,其中肠上皮来源的血清素成为连接肠道与Kupffer细胞介导的IDS清除之间的关键信使。血清素通过作用于Kupffer细胞上的特定受体,触发细胞骨架重塑并上调与吞噬相关的基因表达,从而广泛增强Kupffer细胞对多种IDS的清除能力。在治疗层面,通过短暂干预血清素信号(如限制血清素生成前体的膳食来源或阻断相关血清素受体)可显著提升IDS的递送效率。短时间的干预窗口即可在多种具有临床相关性的IDS治疗中获得显著的治疗获益。
本研究揭示了由共生菌驱动的肠道-肝脏免疫轴是调控IDS清除和系统递送效率的关键机制,提供了直接证据表明,通过调节内源性生物通路可以突破药物递送领域长期存在的屏障。从转化医学角度看,靶向色氨酸代谢或血清素信号通路,为通过减少快速肝脏清除或降低肝毒性来提升IDS递送效果提供了一种具有广泛适用性的策略,对基因治疗、mRNA疗法及精准肿瘤治疗具有重要前景。
中国科大生命科学与医学部王育才、朱书、蒋为教授为本研究的通讯作者,中国科大王育才与蒋为实验室汪沁博士、陈子琦博士和朱书实验室张国荣博士为文章共同一作。
原文链接:https://www.science.org/doi/10.1126/science.adu7686
