I 类内含子(Group I introns)作为最早发现的催化RNA之一,其自剪接与环化能力不仅是生命起源研究的重要线索,也构成了环状RNA(circRNAs)体外合成的重要基础。然而,包含完整外显子序列的全长核酶结构及其自剪接与环化过程的动态调控机制仍有待进一步阐明。

2026年4月14日,中国科学技术大学生医部张凯铭/李珊珊团队在 Nature Chemical Biology期刊上发表题为“Self-splicing and cyclization mechanisms of the full-length Anabaena pre-tRNA”的研究论文, 利用单颗粒冷冻电镜技术捕捉了蓝细菌鱼腥藻(Anabaena sp. PCC 7120)tRNA(Leu) 前体在自剪接与环化过程中的多个关键构象状态,系统揭示了其结构动态机制,并在此基础上实现了环化效率的结构指导优化。同时,该工作受邀配发Research Briefing(“Structural snapshots of self-splicing and circularization of the Anabaena precursor tRNA”),对研究的核心发现进行进一步解读。该研究也是团队在核酶结构与机制研究方向上的又一重要进展(Nature 2021;PNAS 2022;Nucleic Acids Research 2023;Nature Communications 2023;Nature 2025;Nature Catalysis 2025;Nature Communications 2026)。
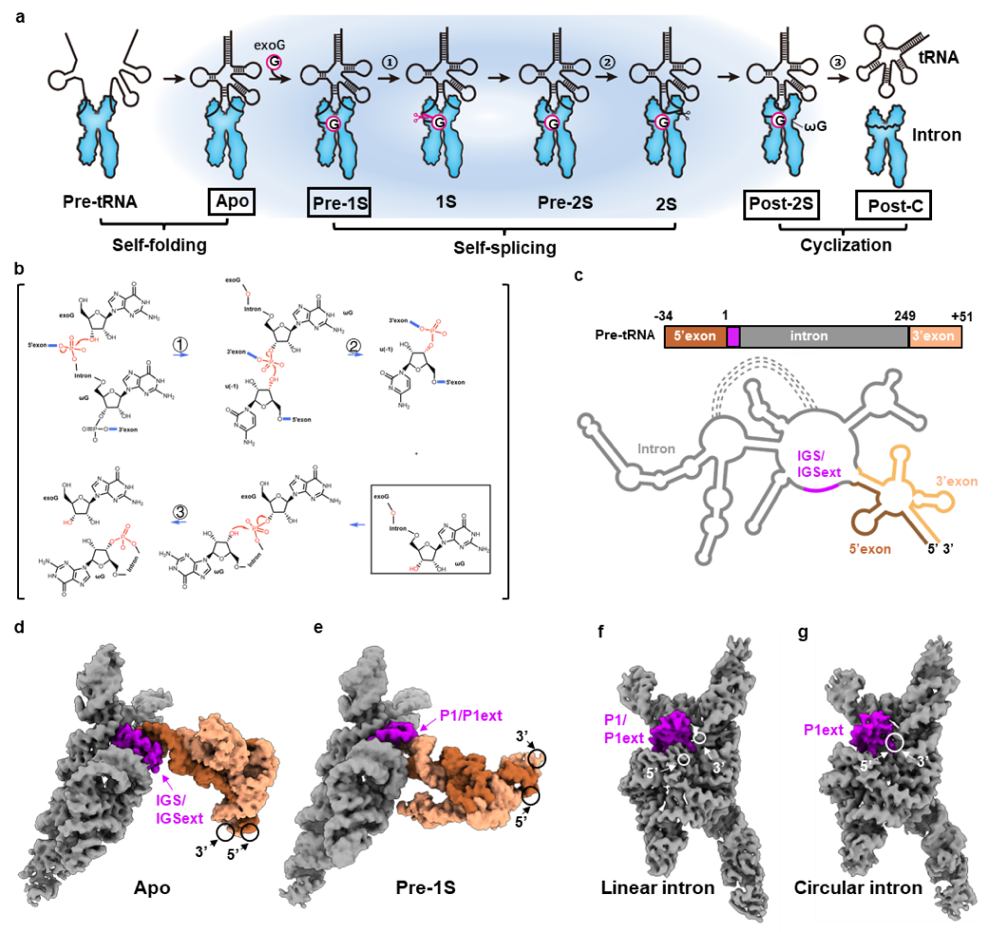
图1:全长Anabaena tRNA(Leu) 前体自剪接与环化的多状态冷冻电镜结构。a. Anabaena tRNA(Leu) 前体催化过程示意图,包括自折叠、自剪接及内含子环化。b. 反应过程中涉及的化学官能团。c. tRNA(Leu) 前体二级结构示意。d-g. tRNA(Leu) 前体的冷冻电镜重构结构。
多状态结构解析:捕捉RNA催化全过程
研究团队通过调控反应条件减缓自剪接过程,并结合硫代磷酸修饰策略,成功捕捉到Anabaena pre-tRNA在不同反应阶段的构象状态,包括Apo、Pre-1S、Pre-2S、线性内含子和环状内含子等多个关键中间体(图1)。结构分析显示,在Apo状态中,尽管P1螺旋尚未形成,tRNA外显子已预先折叠为成熟的“L”形结构,为后续剪接反应提供了结构基础。这一结果揭示了外显子结构在剪接启动中的关键作用。
剪接启动:大尺度结构重排驱动催化
从Apo到Pre-1S状态,RNA发生显著构象变化:tRNA结构域发生了约18 Å的平移与180°的旋转,P1/P1ext螺旋形成,P2螺旋发生约8 Å位移,J9.0/AC-arm从69°扩展至144°,为P1螺旋进入活性中心让出空间。与此同时,G结合口袋(G binding site)与J8/7区域重排,形成了可以容纳外源鸟苷(exoG)的催化环境。值得注意的是,此时exoG虽已结合,其O3'与剪接位点距离接近,但攻击角度尚未达到催化要求,表明Pre-1S状态为一个“预反应”构象,需要进一步微调才能启动第一步剪接反应。
无损环化机制:同一活性位点再利用
与Tetrahymena、Azoarcus、T4 td等I类内含子在环化过程中会丢失若干5' 末端核苷酸不同,Anabaena内含子可在不丢失任何序列的情况下形成完整环状RNA。通过RNase R消化、测序与电泳迁移率分析,研究团队证实了其形成的环状内含子为共价闭合、无额外残基插入的完整环状RNA。线性与环化内含子的结构比对显示,两者整体构象高度相似,表明G结合位点被再次用于环化反应,即ωG的3'-OH发起第三次亲核攻击完成环化。这一发现揭示了核酶通过“复用”同一催化中心实现不同反应步骤的机制,为理解RNA催化的灵活性提供了新的结构依据。
关键位点G37:调控环化效率的分子开关
研究团队进一步发现,位于J2/3区域的G37在环化过程中发生了显著的构象翻转,通过碱基堆积稳定P1延伸结构,从而精准定位环化位点。与此同时,保守的A1–U8碱基对及其与wobble受体基序(A57/A84)的相互作用共同参与环化位点的确定。基于这一结构机制,研究团队对G37进行单点突变(G37U、G37C),在三种不同的环化体系中均显著提高了环化效率。在与最新TRIC-V2方法的对比中,结构优化后的Anabaena PIE系统在最终产率上表现出更高优势。
金属离子动态重排:催化过程的精细调控
作为经典金属酶,I类内含子活性依赖于多个金属离子(MA、MB/C、ME)的精准定位。本研究发现,在不同反应阶段,MA、MB/C、ME等金属离子在活性中心附近发生动态重排:从Apo状态下远离活性位点,到线性内含子中逐渐接近并参与配位,再到环化后重新调整位置。这些变化反映了催化过程中金属离子对反应空间构型的精细调控,进一步揭示了RNA催化的分子基础。
从机制到应用:推动环状RNA技术发展
本研究不仅揭示了Anabaena I类内含子自剪接与环化的结构动态机制,还首次得到了全长内含子序列环化的结构基础,并基于G37及其PIE系统的等位突变实现了环化效率的结构指导性优化(图2)。这些成果不仅加深了对RNA催化机制的理解,也为环状RNA的体外合成、RNA药物开发及相关生物技术应用提供了新的结构设计思路。
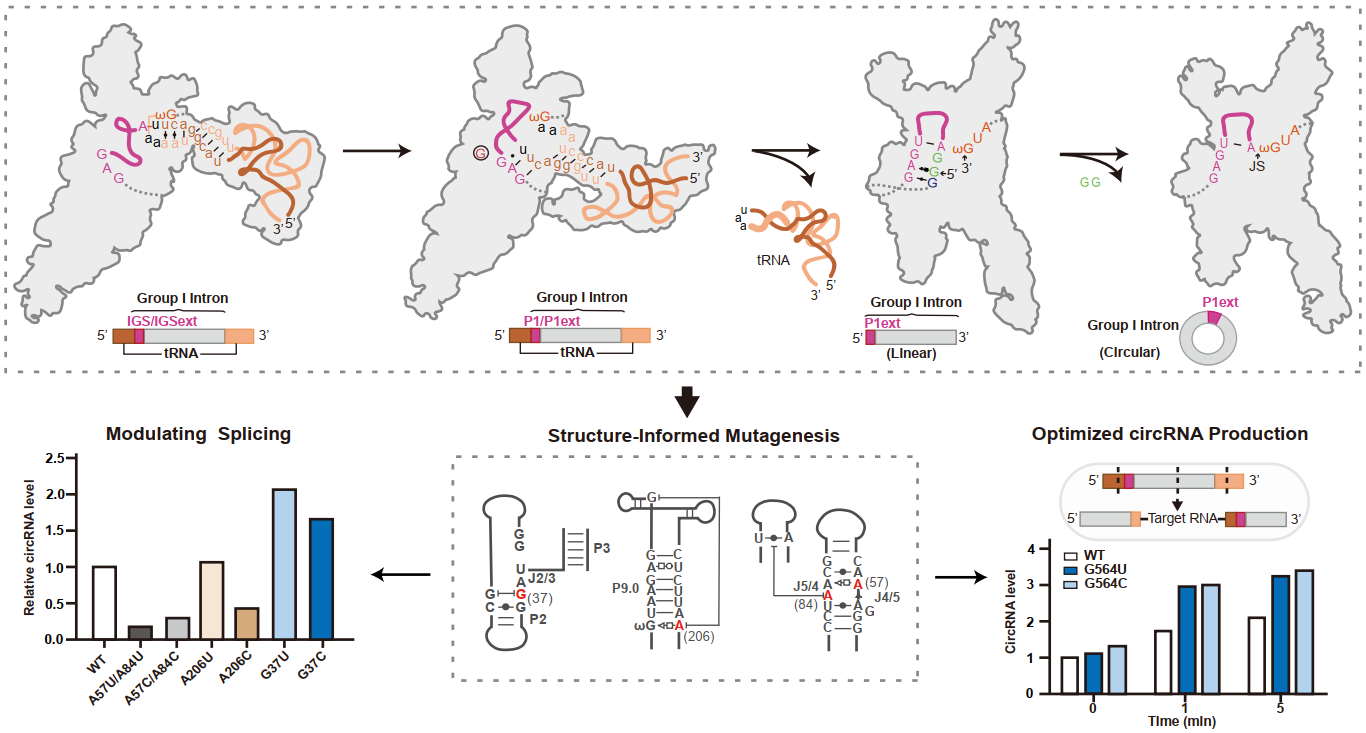
图2:鱼腥藻内含子自剪接与环化的多状态构象及PIE优化应用
该研究工作获得了国家自然科学基金、国家重点研发计划、中国科学院战略性先导科技专项及国际合作项目,以及合肥综合性国家科学中心大健康研究院等项目的资助,并得到细胞动力学教育部重点实验室、中国科学技术大学冷冻电镜中心及附属第一医院、复旦大学电镜中心的大力支持。中国科学技术大学生医部博士研究生张晓静为本文的第一作者,博士生安林凤、伊然、刘霁和博士后杨雯在本研究中做出了重要贡献,李珊珊副教授和张凯铭教授为本文的共同通讯作者。
原文链接:
https://www.nature.com/articles/s41589-026-02205-1
